量化計算中:過渡態理論的起源和意義
我們在化學反應式中看到的變化,往往只是從反應物到產物的一條簡潔箭頭。但在這條箭頭的背后,分子內部究竟經歷了怎樣的結構重組和能量轉化?為什么有些反應能在常溫下迅速完成,而有些卻需要高溫高壓?為什么催化劑能顯著降低反應活化能?又為什么某些反應會產生特定的構型或對映體?這些問題的答案,都隱藏在化學反應最關鍵、最短暫的一個瞬間——那就是過渡態(Transition State)。要真正理解反應機理,我們必須走進過渡態理論。它不僅揭示了反應的“能量路徑”,更讓我們在分子層面上看清化學反應的本質。
一、什么是“過渡態”?
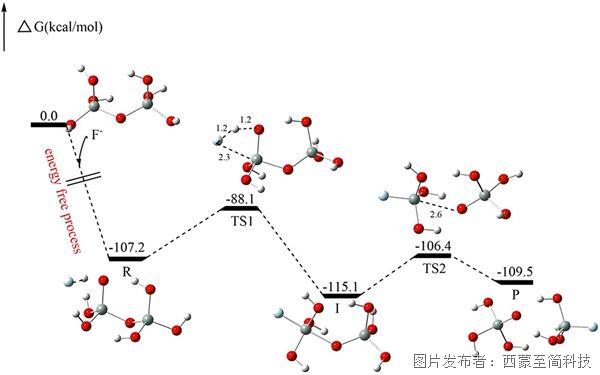
過渡態理論(Transition State Theory, TST)是由物理化學家 Henry Eyring、Michael Polanyi 等人于 1935 年提出,是化學反應動力學領域最具影響力的理論之一,為理解化學反應的本質提供了重要的理論框架。從分子微觀運動的角度,TST首次定量地描述了化學反應過程中分子體系的能量變化和結構重組過程,標志著化學動力學研究從宏觀描述向微觀機理闡釋的重要轉變。
根據該理論,任何化學反應的發生都伴隨著反應勢能面的連續變化,反應物分子必須沿著特定的反應坐標(reaction coordinate)經歷一系列結構重組和能量變化。在此過程中,體系的勢能首先逐步升高,達到一個能量極大值點,這個對應于勢能面上鞍點(saddle point)的結構就是——過渡態(Transition State, TS),又稱 活化絡合物(activated complex)。
二、實例說明
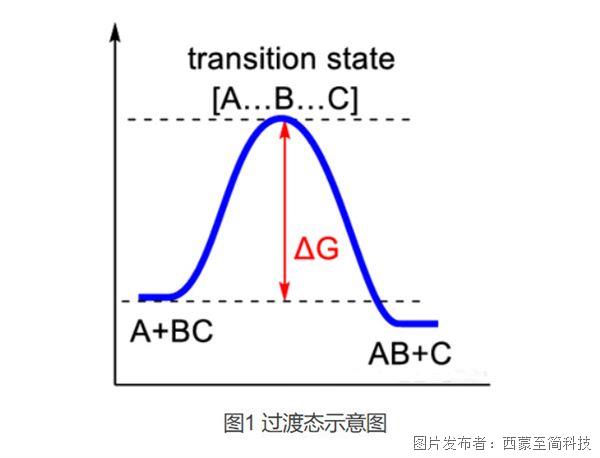
以典型的雙分子置換反應
A + BC → AB + C 為例(圖1),
該理論詳細闡釋了反應的具體過程:
當反應物 A 分子逐漸接近 BC 分子時,
B–C 鍵開始弱化,同時 A–B 鍵開始形成。
當體系達到 [A···B···C] 三中心過渡態 時,
原有的 B–C 鍵 和新生的 A–B 鍵 都處于部分成鍵狀態。
這一過渡態結構處于勢能面的鞍點位置,
之后體系沿著反應坐標繼續演化,
最終完成 B–C 鍵的斷裂 和 A–B 鍵的形成,
得到產物 AB 和 C。
三、計算流程
目前對過渡態的研究主要通過量子化學計算模擬的手段來獲得過渡態的相關信息,而常用的軟件有 Gaussian、ORCA、VASP、CP2K 等。下面以 Gaussian 為例,介紹搜索過渡態的一般流程:
1?? 對反應體系的機理有初步的認知,形成反應機理的猜測。
例如可能的反應機理,以及可能涉及的中間體和過渡態結構。
2?? 使用 GaussView 建立結構模型,并選擇合理的泛函和基組進行中間體的結構優化計算。
3?? 在中間體的基礎上調整結構,編輯 .gjf文件的命令行,使Gaussian 用 TS 方法搜索過渡態(下圖案例)。
4?? 查看過渡態結構以及頻率、振動模式是否符合預期。

圖2 Gaussian計算過渡態的gjf輸入文件
初學者需要注意的是,各個關鍵詞的意義:
nprocshared:代表并行核數;
mem:代表分配的內存大小(32位 Windows 版 Gaussian 一般只支持 4 核并行,1500MB 內存,而 Linux 版則無限制);
calcfc:代表精確計算初始結構的 Hessian 矩陣;
noeigentest:代表優化過程中不對每一步做 Hessian 矩陣本征值數目的檢測;
freq:代表在計算完成后自動進行頻率計算。
四、總結
過渡態理論的提出,使我們得以從分子層面理解化學反應的真正本質。化學反應并非簡單的“反應物變為產物”,而是分子體系在勢能面上沿著反應坐標不斷演化的動態過程。過渡態作為反應勢能的最高點,決定了反應能否發生、速率快慢以及立體選擇性。借助量子化學計算,我們能夠在微觀層面上識別過渡態的幾何結構、能量特征和振動模式,從而深入揭示反應機理與催化本質。可以說,過渡態不僅是化學反應的“能量關口”,更是連接實驗化學與理論化學的橋梁,是理解化學世界的關鍵鑰匙。
提交
有限元仿真中的穩態和瞬態是怎么回事?
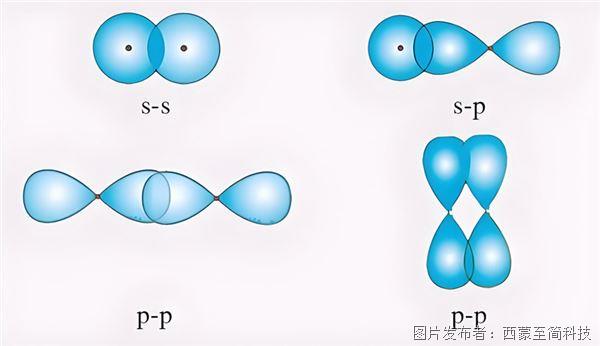
量子化學中的價鍵理論
量子化學:材料的電子態密度
VASP最全入門干貨:四個輸入文件詳解
量子化學:什么是自旋軌道耦合?








 投訴建議
投訴建議